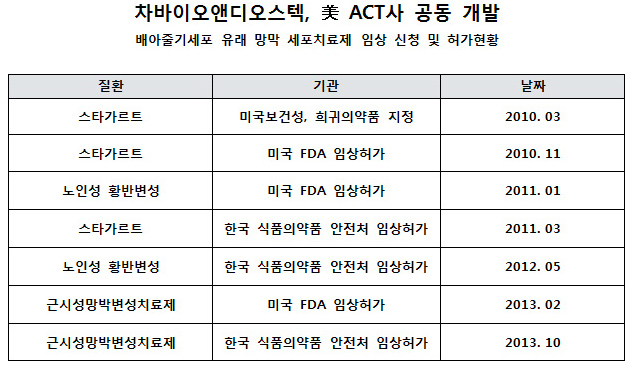
차바이오앤디오스텍,『근시성 망막 황반변성 세포치료제』식약처 임상승인
- 2013.10.29
 |
|||
|
|||
차바이오앤과 협력사인 미 ACT社는 이미 망막줄기세포치료제(RPE)로 희귀질환인 스타가르트(SMD)와 노인성황반변성(AMD)에 대해 美FDA와 한국 식약처에 임상 승인을 받고 한국과 미국, 영국에서 총 28명의 시술을 완료 하였으며, 세번째 적응증인 근시성 망막황반변성에 대한 안전성과 내약성을 평가하는 1/2a임상시험의 피험자 모집을 시작할 예정이다. 현재까지 국내에서 스타가르트(SMD)와 노인성황반변성(AMD) 임상시험 시 이식 받은 피험자에게 이식된 세포의 과도한 증식이나 종양 및 이상조직형성 등 중대한 이상 반응은 없었다. 한편 미국의 ACT (Advanced Cell Technology)社는 지난 5월 배아줄기세포 유래 망막색소상피세포 (ESC-RPE-MMD)를 이식 받은 피험자의 시력이 개선되고 있다고 美 로이트 통신을 통해 임상 중 간결과를 발표 하기도 했다. 전 세계적으로 배아줄기세포를 이용하여 임상 허가를 받아 진행 중인 줄기세포 회사는 현재 차바 이오앤 과 미국 ACT社가 유일하다. 차바이오앤은 국내에서 RPE Cell을 생산할 수 있는 설비와 기술을 갖추었고 타 줄기세포치료제에 비해 임상시험기간이 비교적 짧아 세계 최초의 배아줄기 세포 세포치료제의 상용화가 가능할 것으로 전망된다. “배아줄기세포 유래 망막색소상피세포”를 이용한 근시성 망막변성치료제 임상시험은 분당차병원에서 진행될 예정이다.
|
|||